| 一、标本的留取及保存
a、标本新鲜:一般在2h以内进行,超过2h,组织将有不同程度的自溶,其抗原或变性消失,或严重弥散。
b、取材部位:除取病灶或含待检抗原部位外,还应取病灶与正常交界处,即所取组织切片中同时应有抗原阳性和阴性区,以形成自身对照。细胞坏死后,不仅抗原弥散或消失,而且常引起非特异着色,干扰观察,因此取材时应尽可能避开坏死区。
c、取材时避免挤压,应使用锋利的刀刃,镊取组织动作要轻。
d、取材后的组织需立刻投于固定剂中(常用福尔马林或4%多聚甲醛)
二、免疫组化实验步骤
1,切片,烤片60℃,1h;
2,脱蜡及复水
二甲苯10min,100%乙醇5min,95%乙醇5min,90%乙醇5min,85%乙醇5min,80%乙醇5min, 75%乙醇5min,60%乙醇5min,50%乙醇5min,30%乙醇5min,自来水1min,双氧水1min;
3,1份30%H2O2加10份蒸馏水,室温10min,蒸馏水洗3次,每次3min;
4,微波修复
将切片浸入0.01M枸橼酸缓冲液,微波中最大火力(98℃-100℃)加热至沸腾,冷却(约5-10min),反复两次;
5,将切片自然冷却至室温,PBS洗涤3次,每次5min;
6,封闭,5%BSA,室温20min,甩去多余液体;
7,滴加一抗,37℃,1h,或者4℃过夜;
8,PBS洗涤3次,每次3min;
9,滴加二抗,37℃,15-30min;
10,PBS洗涤3次,每次3min;
11,滴加SABC,37℃, 30min;
12,PBS洗涤3次,每次5min;
13,1ml蒸馏水中分别滴加显色剂,混匀;
14,DAB显色剂配置好后,滴加于切片,室温,镜下检测反应时间(约5min);
15,自来水冲洗干净,过蒸馏水;
16,苏木素复染2min,自来水冲洗;
17,脱水
30%乙醇3min,50%乙醇3min,70%乙醇3min,80%乙醇3min,90%乙醇3min,95%乙醇3min,100%乙醇3min,二甲苯20min;
18,树胶封片,镜检。
三、免疫组化切片保存
采用蜡封固切片和-20度低温保存组织切片来避免抗原损失,或石蜡组织块4度保存
四、优质染色切片的标准
1、图像清晰
2、背景染色浅而特异性染色较深
3、阳性与阴性对照明显。
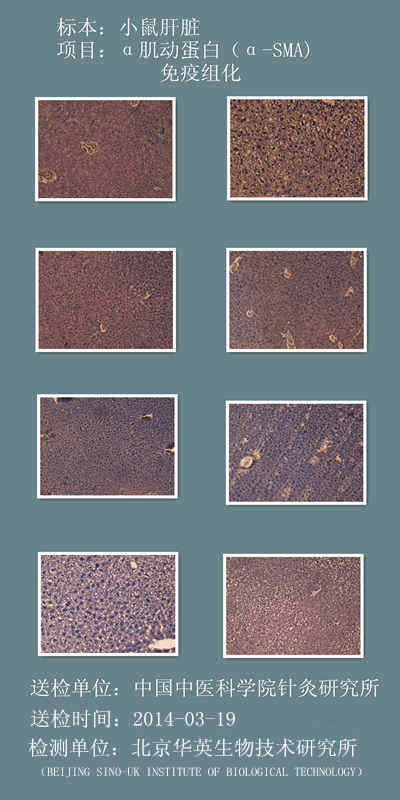
以下是优质切片范例:
|